
Innehåll
I den här artikeln: Använda en pH-mätare Använda solrospapper inklusive pH8-referenser
Det är viktigt att analysera vattnets pH (dvs dess surhetsgrad eller alkalitet). Vatten konsumeras av de växter och djur vi är beroende av och vi konsumerar det direkt varje dag. Vattnets pH kan ge ledtrådar till potentiell förorening. Därför är vatten-pH-analys ett viktigt folkhälsomått.
stadier
Metod 1 Använda en pH-mätare
-

Kalibrera sonden och mätaren enligt tillverkarens anvisningar. För att kalibrera den kan du behöva testa mätaren med ett känt pH-ämne. Du kan sedan justera det baserat på dessa mätningar. Om du ska analysera vatten utanför ett laboratorium bör du utföra kalibreringen innan du skadar enheten i fältet.- Skölj sonden med rent vatten innan du använder den. Torka den med en ren trasa.
-

Samla ett vattenprov i en ren behållare.- Vattenprovet bör vara tillräckligt djupt för att elektrodspetsen ska täckas.
- Låt provet vila ett tag så att temperaturen har tid att stabilisera.
- Mät provets temperatur med en termometer.
-

Ställ in mätaren enligt provets temperatur. Sondens känslighet påverkas av vattentemperaturen och den angivna mätningen kanske inte är bra om du inte anger temperaturdata. -

Placera sonden i provet. Vänta tills mätaren balanserar. Detta uppnås när mätningen förblir stabil. -

Läs provets pH-mätning. Din pH-mätare ska ge dig en mätning på en skala från 0-14. Om vattnet är rent bör mätningen vara nära 7. Skriv ner dina poster.
Metod 2 Använd solrospapper
-

Lär dig skillnaden mellan pH-papper och solrospapper. För att få en korrekt mätning av en lösning kan du använda pH-papper. Det bör inte förväxlas med det nuvarande solrospapperet. Båda kan användas för att analysera syror och baser, men de är radikalt olika.- PH-banden innehåller en serie indikatorkolumner som ändrar färg efter att de utsatts för en lösning. Intensiteten för syrorna och baserna i varje kolumn skiljer sig. När de har ändrats kan färgerna jämföras med exemplen i satsen.
- Solrospappret består av pappersremsor som innehåller en syra eller bas (alkaliskt). De är röda för det mesta (om de innehåller en syra som reagerar med baserna) eller blå (om de innehåller en bas som reagerar med syror). De röda banden blir blå om ämnet är alkaliskt, de blå bandet blir röda om de är i kontakt med en syra.Solrospapper kan användas för snabb och enkel mätning, men de billigare tillåter inte nödvändigtvis noggrann mätning av lösningens pH.
-

Samla ett vattenprov i en ren behållare. Provet ska vara tillräckligt djupt för att tejpen ska täckas. -

Doppa en pappersremsa i ditt prov. Några sekunders exponering borde räcka. De olika kolumnerna på papperet börjar ändra färg om några ögonblick. -

Jämför slutet på analysbandet med den färgade grafen som medföljer papperet. Färgerna i diagrammet ska matcha de i ditt band. Varje färg bör associeras med en pH-mätning.
Metod 3 Förstå pH
-
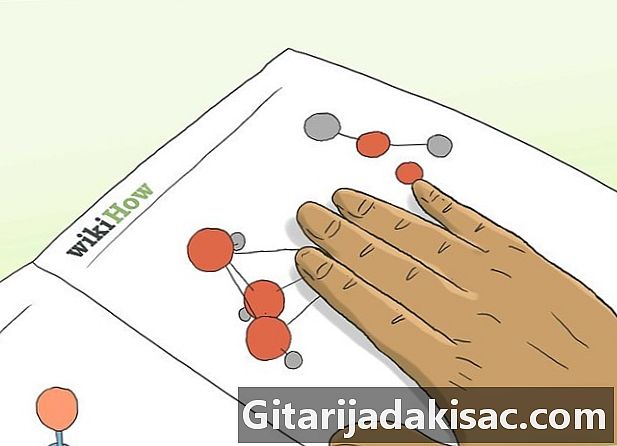
Upptäck hur syror och baser definieras. Laciditet och alkalinitet (termen som används för att beskriva baserna) definieras båda av vätejonerna som de förlorar eller accepterar. En syra är ett ämne som förlorar (eller enligt vissa ger) vätejoner. -
Förstå pH-skalan. PH-talet används för att utvärdera surhetsgraden eller alkaliniteten hos vattenlösliga substanser. Vatten innehåller normalt ett motsvarande antal hydroxid- (OH-) och hydronium (H30 +) -joner. När en sur eller alkalisk substans tillsätts i vatten, ändrar den andelen hydroxid- och hydroniumjoner.- Detta antal är vanligtvis på en skala från 0 till 14 (även om vissa ämnen faktiskt kan överskrida detta intervall). Neutrala ämnen har ett pH nära 7, sura ämnen under 7 och alkaliska ämnen över 7.
- PH-skalan är logaritmisk, vilket innebär att en skillnad på en enhet faktiskt är en tio gånger större skillnad i surhet eller alkalitet. Till exempel är ett ämne med ett pH av 2 faktiskt 10 gånger surare än ett ämne vars pH är 3 och 100 gånger surare än ett ämne med ett pH av 4. Skalan fungerar på samma sätt för alkaliska ämnen, en måttenhet motsvarande en tiofaldig skillnad.
-

Vet varför vi vill mäta pH i vattnet. Rent vatten bör ha ett pH på 7, men kranvatten har vanligtvis ett pH mellan 5,5 och 6. Mycket surt vatten (med lågt pH) är mer benägna att lösa giftiga produkter. Dessa kan förorena vattnet och göra det olämpligt för livsmedel.- Det är allmänt föredraget att mäta pH in situ. Om du samlar in ett vattenprov för studier i ett laboratorium, kan koldioxiden i vattnet lösa sig i vattnet. Denna upplösta koldioxid reagerar med jonerna i vattnet och ökar surheten hos de basiska eller neutrala lösningarna. För att undvika koldioxidföroreningar bör du mäta ditt vatten mindre än 2 timmar efter att du har samlats in.